Hukum Faraday: Penerapan Dan Contoh Soal – Hukum Faraday menjelaskan tentang hubungan proses kimia dengan energi listrik. Proses ini sudah banyak dikenal diberbagai industri sebagai proses elektrolisis, yaitu proses perpindahan muatan listrik pada suatu larutan yang menghasilkan proses kimia pada larutan tersebut.
Hukum Faraday ini dirumuskan dengan : W = e.F
Dengan :
W = massa zat hasil elektrolisis (gram)
E = berat ekuivalen zat hasil elektrolisis
F = jumlah arus listrik dalam satuan Faraday.
Michael Faraday adalah ahli kimia dan fisika yang mempelajari aspek kuantitatif dan kualitatif dari elektrolisis. Ia menemukan hubungan antara massa zat yang dihasilkan di elektrode dengan jumlah listrik yang digunakan.
Michael Faraday melaporkan juga hasil percobaannya tentang muatan listrik melalui gas- gas. Ia menggunakan alat yang menggunakan tabung gelas dan elektroda diujung-ujungnya. Lempeng logam yang disebut elektroda ditempatkan diujung tabung gelas yang divakumkan (hampa), sehingga arus listrik dapat melewati ruang tersebut.
Salah satu elektroda disebut katoda, dihubungkan dengan sumberlistrik negatif dengan tegangan tinggi (beberapa ribu volts), sedang yang lain disebut anoda (kutub posotif). Dari percobaan Faraday dikembangkan oleh Rontgen yang memberikan pengaruh sinar katoda pada suatu permukaan menghasilkan suatu jenis radiasi. Radiasi yang dihasilkan ini yang sekarang dikenal dengan sinar X.
Michael Faraday menerangkan hubungan kuantitatif antara banyaknya arus listrik yang digunakan pada elektrolisis dengan hasil elektrolisisnya dengan gambar 1.
Baca juga: Penjelasan Hukum Kirchoff Secara Lengkap
Daftar isi
Hukum Faraday Listrik
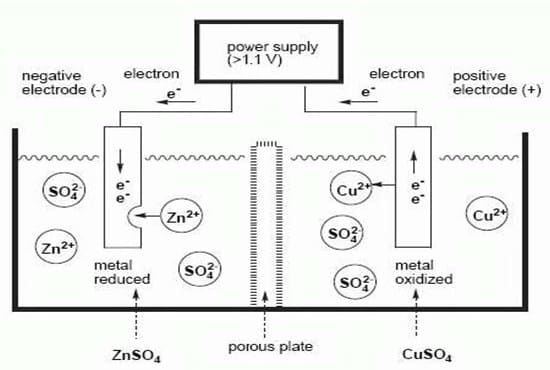
Proses elektrolisis dimulai dengan dialirkannya arus listrik dari baterai. Elektron dari kutub negative mengalir menuju ke katoda. Akibatnya, ion positif Cu2+ dalam lelehan akan tertarik ke katoda. Cu2+ akan tertarik ke katoda dan menyerap elektron untuk tereduksi menjadi logam Cu yang netral.
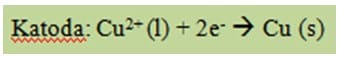
Sementara itu ion negative Cl- dalam lelehan akan tertarik ke anoda. Ion Cl- akan teroksidasi menjadi logam Cl yang netral dengan melepas elektron. Elektron inilah yang akan diambil oleh anoda untuk diteruskan kembali ke kutub positif baterai.
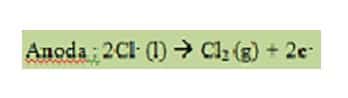
Jadi reaksi redoks yang terjadi pada sel elektrolisis di atas dapat ditulis sebagai berikut:
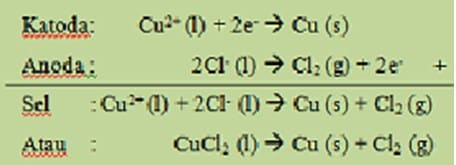
Percobaan Faraday
Setelah Oersted memperlihatkan di tahun 1820 bahwa sebuah arus listrik dapat mempengaruhi jarum sebuah kompas, Faraday menarik hipotesis bahwa jika sebuah arus dapat menghasilkan medan magnet, maka sebaliknya sebuah medan magnet pun dapat menghasilkan arus. Konsep “medan” pada saat itu belum dikenal, dan sasaran Faraday adalah membuktikan bahwa sebuah arus dapat dihasilkan dari “magnetisme”.
Ia berkutat seputar permasalahan ini secara putus-sambung selama periode waktu10 tahun, hingga akhirnya berhasil tahun 1981. Ia melilitkan dua kumparan yang terpisah ke ujung –ujung kumparan sebuah inti toroida besi yang sama, kemudian menyambungkan sebuah galvanometer ke ujung-ujung kumparan yang satu membentuk rangkaian tertutup pertama dan sebuah baterai ke ujung-ujung kumparan lainnya membenuk rangkaian tertutup kedua.
Sejenak setelah rangkaian yang tersambung ke baterai ditutup, Faraday memperhatikan terjadinya penyimpangan sesaat pada jarum galvanometer. Penyimpangan serupa ke arah yang berlawanan terjadi ketika baterai dilepaskan dari rangkaian. Percobaan ini adalah eksperimen pertamanya yang melibatkan medan magnet yang berubah arah, dan hal ini diikuti oleh pembuktian Faraday bahwa sebuah medan magnet bergerak atau sebuah kumparan bergerak juga akan mengakibatkan simpangan pada jarum galvanometer.
Baca juga: Sinar Gamma: Pengertian, Sejarah, Manfaat
Karena arus yang ditimbulkan disebabkan oleh induksi maka arus tersebut dinamakan sebagai arus induksi. Sedangkan induksi yang menyebabkan arus induksi disebut induksi elektromagnetik.
Arah arus induksi dapat ditentukan dengan menggunakan Hukum Lorentz yang berbunyi:
Arah arus induksi di dalam suatu penghantar selalu demikian sehingga menghasilkan medan magnet yang menentang perubahan garis gaya atau sebab-sebab yang menimbulkannya.
Sehingga:
- Jika kumparan didekati dengan kutub Utara magnet, maka terjadi arus induksi yang arahnya berlawanan dengan arah putaran jarum jam.
- Jika kutub Utara medan magnet dijauhikan dari kumparan, maka arah arus induksinya sama dengan arah putaran jarum jam.
- Jika jumlah garis gaya magnet yang masuk ke dalam kumparan berubah-ubah banyaknya, maka akan terjadi beda potensial antara ujung-ujung kumparan. Beda tegangan yang demikian dinamakan gaya gerak listrik induksi ( GGL induksi) dan arus yang terjadi disebut arus induksi atau arus imbas.
Hukum Faraday
Dalam konteks medan, kita dapat mengatakan bahwa sebuah medan magnet yang berubah terhadap waktu akan menghasilkan sebuah gaya gerak listrik (ggl), yang pada gilirannya akan membangkitkan arus jika terdapat sebuah rangkaian tertutup yang memadai. Gaya gerak listrik pada dasarnya adalah tegangan yang timbul karena pergerakan konduktor berarus di dalam sebuah medan magnet, atau karena adanya medan yang berubah-ubah.
Hukum Faraday yang berbunyi:
GGL induksi yang timbul antara ujung-ujung suatu loop penghantar berbanding lurus dengan laju perubahan fluks magnetik yang dilingkupi oleh loop penghantar tersebut.
Hubungan tersebut dinyatakan dengan dua hukum Faraday. Untuk memahami hukum tersebut, akan digunakan istilah mol elektron dan satu faraday. Lalu apa itu mol elektron dan satu faraday?
Di dalam reaksi reduksi dan oksidasi pada elektrolisis terjadi transfer elektron. Sebagai contoh, pada reaksi reduksi Cu2+, ion Cu2+ dalam lelehan menerima arus listrik (elektron) dari luar untuk membentuk Cu(s).
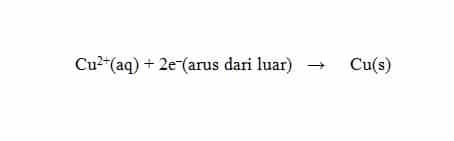
Dikatakan:
- Untuk menghasilkan 1 mol logam Cu, diperlukan 2 mol elektron.
- Untuk menghasilkan 2 mol logam Cu, diperlukan 4 mol elektron.
- Untuk menghasilkan 3 mol logam Cu, diperlukan 6 mol elektron, dan seterusnya.
Jika kita mengetahui jumlah mol elektron yang dibutuhkan, lalu bagaimana menghitung jumlah listrik yang diperlukan?
Secara eksperimen telah diperoleh bahwa 1 mol elektron mengandung muatan listrik sebesar 96.500 coulomb. Untuk menghormati Michael Faraday, 1 mol elektron disebut juga sebagai satu faraday (1F).
1 mol elektron = 1 faraday
1 mol elektron atau 1 faraday menganddung muatan listrik 96.500 coulomb.
Dengan demikian untuk reaksi di atas dapat disimpulkan:
- Untuk menghasilkan 1 mol logam Cu, diperlukan muatan listrik 2 x 96.500 coulomb.
- Untuk menghasilkan 2 mol logam Cu, diperlukan muatan listrik 4 x 96.500 coulomb.
- Untuk menghasilkan 3 mol logam Cu, diperlukan muatan listrik 6 x 96.500 coulomb.
Jadi, muatan listrik (Q) yang dibutuhkan berbanding lurus dengan mol elektron, dan dirumuskan sebagai berikut: Q = n F
Dengan n = jumlah mol elektron (mol), F = muatan listrik per 1 mol elektron (coulomb /mol).
Dari penjelasan di atas, kita sekarang dapat mengaitkan hubungan antara massa zat yang terbentuk pada elektrode dengan jumlah listrik yang digunakan. Inilah yang disebut dengan Hukum Faraday 1.
Hukum Faraday 1
Massa zat yang dihasilkan pada suatu elektrode selama proses elektrolisis berbanding lurus dengan muatan listrik yang digunakan.
Kita sudah mengetahui bahwa massa zat (w) yang dihasilkan pada elektrode berbanding lurus dengan jumlah molelektron. Sementara, jumlah mol elektron berbanding lurus dengan muatan listrik (Q) dalam elektron. Jadi, dapat disimpulkan:

Dengan Q menunjukan besarnya muatan listrik di suatu titik di kawat jika arus listrik I ampere melewatinya selama t detik. Secara matematis:
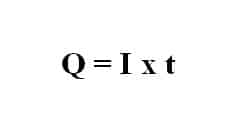
Dengan I = arus listrik (ampere) dan t = waktu (detik). Sehingga, persamaan di atas dapat ditulis menjadi:
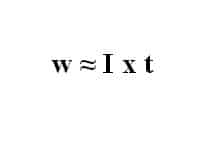
Hukum Faraday 2
Massa zat yang dihasilkan pada elektrode berbanding lurus dengan massa ekivalen zat. Di dalam hukum Faraday 2 dinyatakan bahwa massa yang dihasilkan pada elektrode berbanding lurus dengan massa ekivalen zat.
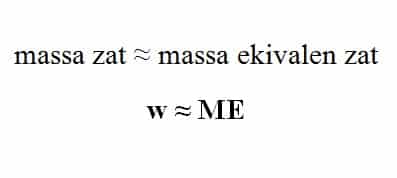
Massa ekivalen zat adalah massa atom relatif (Ar) dibagi dengan perubahan bilangan oksidasinya atau muatan ionnya.
ME = Ar/biloks atau muatan ion
Gaya Gerak Listrik Induksi (GGL) Induksi
Sebuah magnet batang yang dililit oleh suatu kawat penghantar, diharapkan pada kawat penghantar ini timbul arus yang nantinya diukur oleh sebuah Galvanometer. Akan tetapi arus yang diharapkan tidak terjadi, dan percobaan ini dianggap gagal. Akan tetapi pada tahun 1821 Faraday dan Henry mengamati hal yang lain, bahwa ketika batang magnet mulai dimasukkan ke dalam lilitan kawat, terjadi arus yang terukur oleh Galvanometer, namun arus tersebut setelah beberapa saat kemudian hilang.
Hal yang sama terjadi ketika batang magnet dikeluarkan dari lilitan. Sehingga Faraday dan Henry mengambil kesimpulan bahwa perubahan medan magnetiklah yang menimbulkan arus listrik, bukan hanya medan magnet. Arus listrik bisa terjadi jika pada ujung-ujung kumparan terdapat GGL (gaya gerak listrik).GGLyang terjadi di ujung-ujung kumparan dinamakan GGL induksi. Arus listrik hanya timbul pada saat magnet bergerak. Jika magnet diam di dalam kumparan, di ujung kumparan tidak terjadi arus listrik. Fenomena perubahan medan magnet yang menimbulkan arus listrik ini dinamakan Induksi Elektromagnetik.
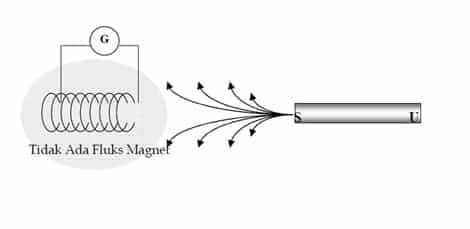
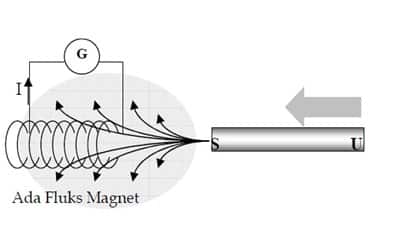
Faktor yang memengaruhi besar GGL Induksi sebenarnya dapat dilihat pada besar kecilnya penyimpangan sudut jarum galvanometer.Jika sudut penyimpangan jarum galvanometer besar, GGL induksi dan arus induksi yang dihasilkan besar.
Ada tiga faktor yang memengaruhi GGL induksi, yaitu :
- Kecepatan gerakan magnet atau kecepatan perubahan jumlah garis-garis gaya magnet (fluks magnetik)
- jumlah lilitan
- medan magnet
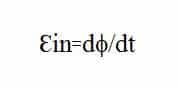
Yang artinya adalah bahwa Gaya Gerak Listrik yang dihasilkan adalah sama dengan negatif dari perubahan fluks magnetik terhadap waktu. Fluks magnetik φ adalah banyaknya garis gaya yang tegak lurus tiap satuan luas A, identik dengan fluks listrik dalam bagian elektrostatik.
Subscript i menunjukkan jumlah lilitan.Tanda negatif berkenaan arah GGL dan induksi magnetik. Jika fluks magnetik yang masih pada kumparan dari medan magnet bertambah, yang artinya magnet didekatkan pada kumparan maka arah arus dari GGL induksi sedemikian sehingga melawan medan magnet.
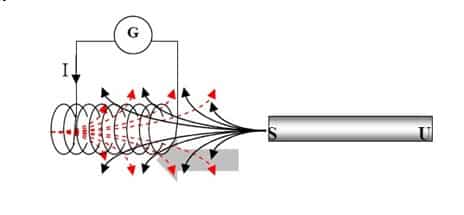
Demikian juga sebaliknya.Untuk kumparan dengan banyak lilitan N, maka GGL induksinya adalah :
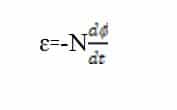
dengan :
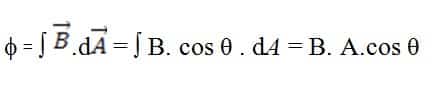
di mana θ adalah sudut antara B dengan A. Jadi GGL induksi terjadi bukan karena adanya medan magnet (B) atau fluks magnetik, akan tetapi karena perubahan fluks magnetiknya.
Penerapan Hukum Faraday Kimia
Penerapan GGL Induksi Hukum Faraday
Pada GGL Induksi sesuai Hukum Faraday terjadi perubahan bentuk energi gerak menjadi energi listrik. Induksi digunakan pada pembangkit energi listrik. Pembangkit energi listrik yang menerapkannya adalah generator dan dinamo. Di dalam generator dan dinamo terdapat kumparan dan magnet.
Kumparan atau magnet yang berputar menyebabkan terjadinya perubahan jumlah garis-garis gaya magnet dalam kumparan. Perubahan tersebut menyebabkan terjadinya GGL induksi pada kumparan. Energi mekanik yang diberikan generator dan dinamo diubah ke dalam bentuk energi gerak rotasi. Hal itu menyebabkan GGL induksi dihasilkan secara terus-menerus dengan pola yang berulang secara periodik.
Generator
Generator dibedakan menjadi dua, yaitu generator arus searah (DC) dan generator arus bolak-balik (AC). Baik generator AC dan generator DC memutar kumparan di dalam medan magnet tetap. Generator AC sering disebut alternator. Arus listrik yang dihasilkan berupa arus bolak-balik.Ciri generator AC menggunakan cincin ganda. Generator arus DC, arus yang dihasilkan berupa arus searah. Ciri generator DC menggunakan cincin belah (komutator). Jadi, generator AC dapat diubah menjadi generator DC dengan cara mengganti cincin ganda dengan sebuah komutator.
Sebuah generator AC kumparan berputar di antara kutub-kutub yang tak sejenis dari dua magnet yang saling berhadapan. Kedua kutub magnet akan menimbulkan medan magnet. Kedua ujung kumparan dihubungkan dengan sikat karbon yang terdapat pada setiap cincin. Kumparan merupakan bagian generator yang berputar (bergerak) disebut rotor. Magnet tetap merupakan bagian generator yang tidak bergerak disebut stator. Ketika kumparan sejajar dengan arah medan magnet (membentuk sudut 0°), belum terjadi arus listrik dan tidak terjadi GGL induksi.
Pada saat kumparan berputar perlahan-lahan, arus dan GGL beranjak naik sampai kumparan membentuk sudut 90°. Saat itu posisi kumparan tegak lurus dengan arah medan magnet. Pada kedudukan ini kuat arus dan GGL induksi menunjukkan nilai maksimum. Selanjutnya, putaran kumparan terus berputar, arus dan GGL makin berkurang. Ketika kumparan membentuk sudut 180 °kedudukan kumparan sejajar dengan arah medan magnet, maka GGL induksi dan arus induksi menjadi nol.
Putaran kumparan berikutnya arus dan tegangan mulai naik lagi dengan arah yang berlawanan. Pada saat membentuk sudut 270°, terjadi lagi kumparan berarus tegak lurus dengan arah medan magnet. Pada kedudukan kuat arus dan GGL induksi menunjukkan nilai maksimum lagi, namun arahnya berbeda. Putaran kumparan selanjutnya, arus dan tegangan turun perlahan-lahan hingga mencapai nol dan kumparan kembali ke posisi semula hingga membentuk sudut 360°.
Dinamo
Dinamo dibedakan menjadi dua yaitu, dinamo arus searah (DC) dan dinamo arus bolak-balik (AC). Prinsip kerja dinamo sama dengan generator yaitu memutar kumparan di dalam medan magnet atau memutar magnet di dalam kumparan. Bagian dinamo yang berputar disebut rotor. Bagian dinamo yang tidak bergerak disebut stator.
Perbedaan antara dinamo DC dengan dinamo AC terletak pada cincin yang digunakan. Pada dinamo arus searah menggunakan satu cincin yang dibelah menjadi dua yang disebut cincin belah (komutator). Cincin ini memungkinkan arus listrik yang dihasilkan pada rangkaian luar dinamo berupa arus searah walaupun di dalam dinamo sendiri menghasilkan arus bolak-balik. Adapun, pada dinamo arus bolak-balik menggunakan cincin ganda (dua cincin).
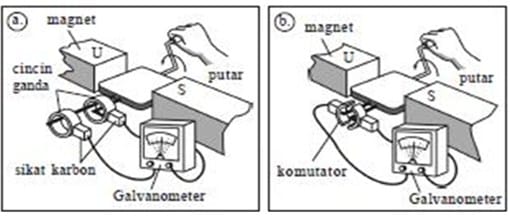
Alat pembangkit listrik arus bolak balik yang paling sederhana adalah dinamo sepeda. Tenaga yang digunakan untuk memutar rotor adalah roda sepeda. Jika roda berputar, kumparan atau magnet ikut semakin cepat gerakan roda sepeda, makin cepat magnet atau kumparan berputar.
Makin besar pula GGL induksi dan arus listrik yang dihasilkan. Jika dihubungkan dengan lampu, nyala lampu makin terang. GGL induksi pada dinamo dapat diperbesar dengan cara putaran roda dipercepat, menggunakan magnet yang kuat (besar), jumlah lilitan diperbanyak, dan menggunakan inti besi lunak di dalam kumparan.
Aplikasi Hukum Faraday dalam mesin listrik
- Generator listrik
Generator listrik adalah alat yang memproduksi energi listrik dari sumber mekanik dengan menggunakan induksi elektromagnetik. Konsep generator pertama kali ditemukan oleh Michael Faraday yang berkebangsaan Inggris, seperti yang ditunjukkan pada gambar di bawah ini.
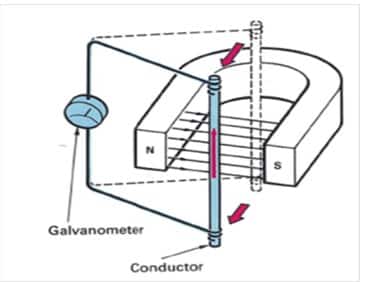
Dari gambar di atas, bila konduktor digerakkan maju mundur antara kutub utara dan kutub selatan maka jarum galvanometer akan bergerak. Gerakan tersebut menunjukkan adanya gaya listrik yang dihasilkan. Dari gambar di atas dapat juga diamati bahwa:
- Jarum Galvanometer akan bergerak, bila konduktor/magnet yang bergerak
- Arah gerak jarum sama dengan arah gerakan konduktor arah kutub-kutubnya
- Besarnya penyimpangan jarum akan sebanding dengan kecepatan potong.
- Jarum tidak akan bergerak bila gerakan dihentikan.
Merumuskan GGL Induksi dalam Hukum Faraday
Faraday merumuskan kesimpulan GGL Induksi ini menjadi sebuah perumusan matematis,
Contoh Soal Hukum Faraday
Tembaga (Cu) mempunyai Ar =63,5. Berapakah massa ekivalen untuk reaksi berikut?
Jawab:
Pada reaksi di atas, perubahan bilangan oksidasinya adalah +2.
Jadi, massa ekivalen Cu adalah: ME = Ar/biloks = 63,5/2 = 31,75
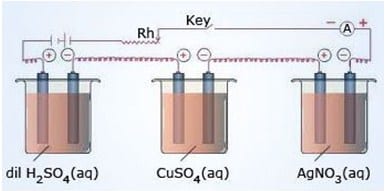
Selanjutnya, jika jumlah listrik sama dialirkan ke dalam dua atau lebih sel elektrolisis dengan elektrolit yang berbeda, maka perbandingan massa zat yang dibebaskan sama dengan perbandingan massa ekivalen zat. Perhatikan gambar di atas, terlihat bahwa jika jumlah listrik yang sama melewati ketiga coulometer, maka massa zat H2, Cu, dan Ag yang dihasilkan akan berbanding lurus dengan massa ekivalennya.
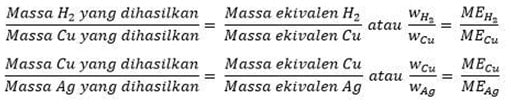
Secara umum, jika terdapat dua macam zat A dan B, maka
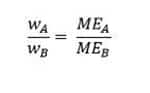
Contoh Soal Hukum Faraday
Jika pada rangkaian di atas terbenttuk endapan Cu sebesar 5 gram, berapakah massa Ag yang mengendap pada elekrode? (Cu = 63,5; Ag = 108).
Jawab:
Untuk menghitung massa Ag, wAg, gunakan rumus:
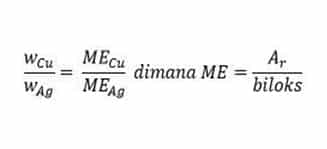
Diketahui massa Cu, wCu = 5 gram
Hitung MECu dan MEAg dengan menulis reaksi reduksi Cu dan Ag.
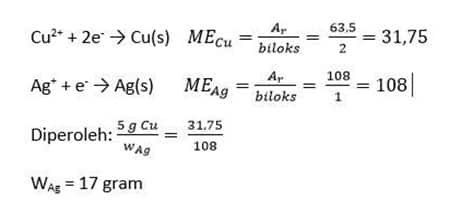
Mari kita lihat kembali Hukum Faraday 1 dan Hukum Faraday 2:
Hukum Faraday 1 : w ≈ I x t
Hukum Faraday 2 : w ≈ ME
Jika digabungkan, kita peroleh w ≈ I x t x ME
Perbandingan ini menjadi persamaan dengan penambahan faktor 1/96.500, sehingga diperoleh rumus hukum faraday :
w = 1/96.500 x I x t x ME
dengan w = massa zat yang dihasilkan (gram)
I = arus listrik (ampere)
t = waktu (detik)
ME = massa ekivalen zat
Contoh Soal Hukum Faraday
Arus listrik 0,2 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan CuCl2. Hitunglah endapan Cu yang terbentuk pada katode. (Ar Cu=63,5)
Jawab:
Hitung endapan Cu, wCu, menggunakan rumus:
wCu = (1/96.500) x I x t x MECu = dimana ME = Ar/biloks
Diketahui:
Arus, I = 0,2 A;
Waktu, t = 50 menit = 50 x 60 detik = 3.000 detik
Cari nilai MECu dengan menuliskan reaksi reduksi Cu:
Cu2+(aq) + 2e– → Cu(s) ; MECu = Ar/biloks = 63,5/2 = 31,75
Jadi, diperoleh:
WCu = (1/96.500) x 0,2 A x 3.000 detik x 31,75 = 0,197 g.
Contoh Soal Kimia
Kimia Study Center – Contoh soal dan pembahasan tentang perhitungan hukum faraday pada elektrolisis SMA kelas 12 IPA.
Soal No.1
Pada elektrolisis larutan ZnSO4 terjadi reduksi Zn2+ menjadi Zn. Massa ekivalen dari Zn adalah….(Ar Zn = 65)
A. 7,5
B. 13,0
C. 15,0
D. 32,5
E. 65,0
Pembahasan
Zn2+ (aq) + 2e → Zn (s)
Massa ekivalen Zn disini adalah Ar dari Zn dibagi dengan biloks atau valensinya .
e = Ar / biloks
e = 65 / 2 = 32,5
Soal No.2
Pada elektrolisis leburan Al2O3 terjadi reduksi Al3+ menjadi Al. Tentukan massa ekivalen dari Al (Ar Al = 27)
Pembahasan
Al3+ + 3e → Al
Massa ekivalen Al
e = 27/ 3
e = 9
Demikian penjelasan artikel diatas semoga dapat bermanfaat bagi semua pembaca setia kami… terimakasih…





Tinggalkan Balasan